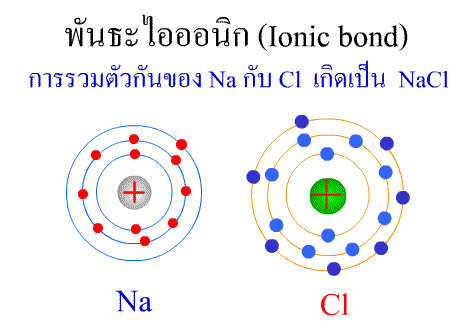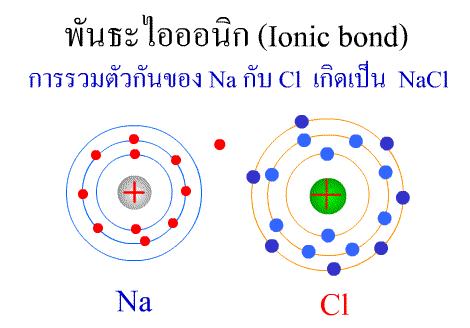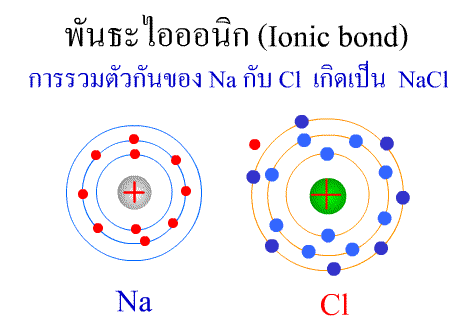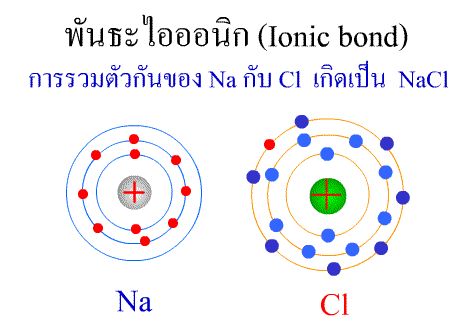
โมลาริตี (molarity : M)
โมลาริตี หรือ โมลาร์ เป็นหน่วยความเข้มข้น ที่เป็นอัตราส่วนของจำนวนโมลของตัวถูกละลายที่อยู่ในสารละลาย ปริมาตร 1 ลิตร (L) จะเขียนแทนด้วยสัญลักษณ์ M สามารถเขียนเป็นสูตรได้ดังนี้
โมลาร์ มีหน่วยเป็น mol / L
ปริมาตรของสารละลาย โดยทั่วไปจะบอกเป็นหน่วยมิลลิลิตร (mL) ดังนั้น ความสัมพันธ์หน่วยของปริมาตร ระหว่าง มิลลิลิตร กับ ลิตร อ่านเพิ่มเติม